合作客戶/
拜耳公司 |
同濟大學 |
聯合大學 |
美國保潔 |
美國強生 |
瑞士羅氏 |
相關新聞Info
-
> 水和乙二醇-水混合體系中的離子液體-陽離子表面活性劑混合膠束自聚焦-電導法 表面張立法和光譜研究法—
> 克服表面張力使液態金屬可拉伸電子器件化的研究進展
> 表面張力的形成同處在液體表面薄層內的分子的特殊受力狀態密切相關。下列現象,與表面張力無關的是:
> 露珠為什么是球形的?這是液體的表面張力造成的!
> 酯功能化的雙子表面活性劑與血紅蛋白的結合——摘要、簡介
> 水面上單分子層膜通過磷脂光控開關實現可逆光學控制:結果和討論、結論
> 氟化石墨烯復合鍍層制備,如何減小電極和鍍液之間的界面張力
> ?白酒掛杯與表面張力有何關系
> 表面張力儀分子所受到的各個方向的力是相同的
> 座滴法測量玻璃熔體表面張力的影響因素研究
膜蛋白穩定技術及其在藥物篩選中的應用進展
來源:藥學學報 瀏覽 1863 次 發布時間:2022-09-20
摘要
膜蛋白承擔了生物膜的主要功能,是新藥研發最重要的靶點群,大約60%的藥物以膜蛋白為靶點。由于膜蛋白在水溶液中有明顯的聚集和變性傾向,在體外很難模擬維持膜蛋白正確構象的類膜環境,導致膜蛋白的結構和功能以及相關配體藥物的研究遠遠滯后于水溶性蛋白。膜蛋白穩定技術對于建立高專屬性、高靈敏度和高通量的膜蛋白配體藥物篩選方法具有重要的意義。本文綜述了目前用于穩定分離純化膜蛋白的一些技術,包括洗滌劑、人造膜、聚合物、慢病毒顆粒等,以及這些技術在藥物篩選中的具體應用。
正文
膜蛋白(membrane proteins,MPs)是細胞膜的重要組成部分,在物質運輸、信號轉導和細胞間識別等多種細胞功能中發揮著重要作用。人類基因組中編碼的MPs約占總蛋白質組的25%。這些MPs與囊性纖維化、動脈粥樣硬化、帕金森病和阿爾茨海默病等多種疾病相關[1]。MPs暴露在細胞外的區域是許多藥物作用的潛在靶點,據估計MPs是60%藥物的靶點[2],如ABC轉運蛋白[3]、核苷轉運蛋白[4]、G蛋白偶聯受體[5]、微囊蛋白-1[6]等。一些MPs可調節細胞反應使藥物直接進入細胞內,或者以通道的形式幫助藥物進入細胞內部發揮藥效;而另一些MPs則主動從細胞中泵出藥物,因此MPs可以極大地影響藥物的治療效果。
作為最具前景的藥物潛在靶點群,MPs的分離純化對于其結構和功能研究以及新藥研發具有重大意義。研究發現MPs需要維持脂質雙分子層或類脂環境才可以保持其天然構象,但是這種環境在體外很難模擬;并且MPs在水溶液中還有明顯的聚集和變性傾向,因此MPs的結構生物學研究十分滯后。目前已知結構的蛋白中只有2%~3%是MPs[7]。此外,MPs的表達量一般都較低,難以被分離純化得到足夠量的目標MPs。如何將MPs分離純化并獲得穩定的結構是MPs研究的難點問題。針對MPs脫離天然膜環境后易聚集和變性的現象,早期研究者提出了以表面活性劑為主的洗滌劑策略,利用其形成的膠束來分離MPs,但在應用過程中存在一些問題[8];進而提出了以脂質體、納米盤等兩親體系來模擬天然膜環境,一定程度上保證了MPs在分離純化過程中構象和功能的完整性[9];近年來還出現了保護MPs周圍局部脂質環境的聚合物穩定技術[10]、慢病毒顆粒穩定技術[11]等。
本文針對MPs穩定技術進行綜述,包括傳統和新型的洗滌劑、人造膜、聚合物、慢病毒顆粒等穩定技術以及其在藥物篩選中的具體應用,為下游MPs結構和功能研究提供可靠的技術支持,促進以MPs為靶點的新藥研發和中藥活性成分的高通量篩選。
01、洗滌劑穩定技術(detergent)
早期的MPs穩定主要采用洗滌劑策略實現。洗滌劑是以表面活性劑為主的一類混合物的統稱,它能降低兩種不混溶液體之間的界面張力[12]。洗滌劑的整體分子結構由親水的極性頭基團和疏水的非極性尾基團組成。水溶液中,細胞膜以脂質雙分子層的形式存在,洗滌劑分子在高于臨界膠束濃度(critical micelle concentration,CMC)時以膠束形式存在。當細胞膜和洗滌劑膠束混合時,洗滌劑分子首先以非協同的方式結合在細胞膜表面,隨著洗滌劑數量的增加,洗滌劑分子從細胞膜表面摻入進脂質雙分子層內部,此時的非協同結合轉變為協同結合,洗滌劑與細胞膜的協同和非協同結合稱為跨雙分子層機制[13]。隨著越來越多的洗滌劑被合并到膜中,脂-洗滌劑混合膠束形成,細胞膜被裂解,洗滌劑成功地提取MPs形成膠束,過程如圖1所示。
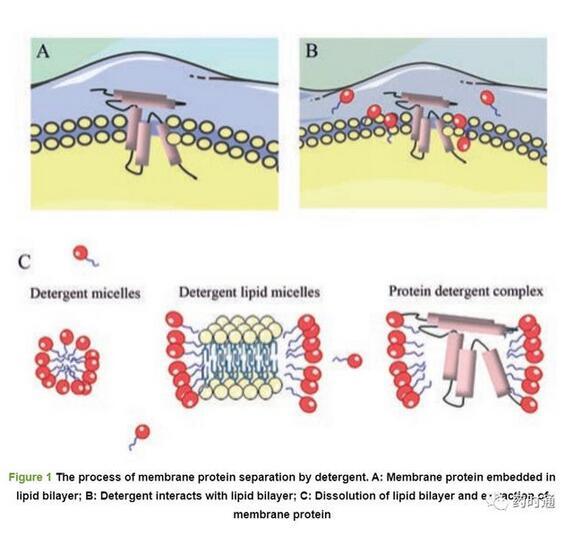
1.1傳統洗滌劑
傳統洗滌劑包括N-辛基-β-D-吡喃葡萄糖苷(N-octyl-β-D-glucopyranoside,OG)、N-癸基-β-D-麥芽糖苷(N-decyl-β-D-maltoside,DM)、N-十二烷基-β-D-麥芽糖苷(N-dodecyl-β-D-maltoside,DDM)、N-壬基-β-D-吡喃葡萄糖苷(N-nonyl-β-D-pyranoglucoside,NG)和月桂基二甲基氧化胺(lauryl dimethylamine oxide,LDAO)。其中DDM作為最經典的洗滌劑,通常是MPs提取的首選洗滌劑[14]。不同洗滌劑對于MPs的分離純化有各自不同的傾向性。Iwata等[15]發現DDM對轉運蛋白和呼吸復合物的分離作用較好,而OG對通道蛋白的分離作用較好。Newstead等[16]發現LDAO會導致大多數的轉運蛋白聚集。Simon等[17]的研究表明DDM、DM、OG、NG對于α螺旋蛋白提取效率相近。有報道[18]稱在LDAO中,電壓依賴性陰離子通道蛋白可保持穩定結構。此外,不同類型的洗滌劑提取MPs時所需的磷酸鹽濃度也不同。Metola等[19]研究發現在較高的磷酸鹽濃度時,兩性離子型洗滌劑LDAO比非離子型洗滌劑DDM有更高的提取效率。不同類型洗滌劑對蛋白的穩定性也不同,據估計只有20%的MPs能在LDAO中維持穩定[20];相比之下,非離子型洗滌劑DDM中大部分蛋白質穩定性明顯優于LDAO,但非離子型洗滌劑的提取效率往往低于兩性離子型洗滌劑。在傳統洗滌劑的應用過程中,研究者們描述的共性問題在于膠束中的MPs穩定性不高,很難保持MPs的天然構象,限制了MPs結構和功能研究及其下游應用。
1.2新型洗滌劑
針對傳統洗滌劑中MPs穩定性不高的問題,研究者開發出一系列新型洗滌劑,主要有:環戊烷基麥芽糖苷、杯芳烴基洗滌劑、不對稱麥芽糖新戊二醇、線性和支化甘露醇基兩親體、三苯基核麥芽糖苷等。它們與傳統洗滌劑相比,能更好地穩定MPs。
Das等[21]制備了一類以環戊烷為核心單元的新型非對映體洗滌劑,即環戊烷基麥芽糖苷(cyclopentyl maltosides,CPMs),并對其穩定幾種模型MPs的能力進行了評價。與常規洗滌劑DDM相比,CPMs對包括兩個G蛋白偶聯受體(G protein-coupled receptors,GPCRs)在內的所有被測MPs表現出更高的穩定性和提取效率。而Hardy等[22]開發的杯芳烴基洗滌劑具有更高的熱穩定性。在杯芳烴基洗滌劑中,MPs能保持穩定的溫度與經典洗滌劑DDM相比至少提高了30℃。Hyoung等[23]制備了一系列的不對稱麥芽糖新戊二醇(neopentyl maltose glycols,NMGs),并對它們的MPs溶解和穩定性能進行評估,包括兩種G蛋白偶聯受體,結果顯示與DDM相比,MNGs對所測的MPs有更高的穩定性。此外還有很多比經典洗滌劑DDM性能更好的洗滌劑,如基于間苯二酚的葡萄糖苷和麥芽糖苷的兩親性洗滌劑[24](分別稱為RGAs和RMAs)、三苯基核麥芽糖苷洗滌劑[25](triphenyl maltosides,TPMs)、錫基肌醇苷洗滌劑[26](tin inositol glycoside,SIGs)等都在一定程度上具有更高的MPs穩定性和提取效率。Hussain等[27]設計合成了線性和支化甘露醇基兩親體(mannitol amphiphilics,MNAs),通過比較研究表明,大多數支化MNAs在MPs穩定性方面都優于線性MNAs。內容由藥時通小編查閱文獻選取,排版與編輯為原創。如轉載,請尊重勞動成果,注明來源于藥時通公眾號。
盡管新型洗滌劑在一定程度上提高了分離純化過程中MPs的穩定性,但新舊洗滌劑都有一些共性的缺陷[28]:①對于未知性質MPs的分離、純化和穩定的洗滌劑選擇,需要進行廣泛篩選;②洗滌劑以形成膠束的形式分離純化MPs,常常會導致MPs失去與脂質和其他蛋白質的天然相互作用;③穩定分離MPs效果好的洗滌劑有時會干擾下游應用。因此,無法預測哪種洗滌劑對給定的蛋白質最有效,需要通過反復實驗來確定。
02、人造膜穩定技術
針對洗滌劑策略的不足,研究者們提出了新的模擬天然膜環境的兩親體系的人造膜策略。該策略的靈感來自新興的納米科學,充分考慮了磷脂雙分子層的復雜性和維持MPs活性的重要性,確保在局部膜環境中穩定地分離純化MPs。人造膜穩定MPs的基本原理是將二油酰基磷脂酰膽堿、二油酰磷脂酰甘油、棕櫚油酰磷脂酰膽堿、膽固醇等細胞膜含有的磷脂類成分,采用不同的反應條件,制備成脂質體、雙胞體和納米圓盤等多種形式,并與純化或重組的MPs按一定比例混合,即可實現MPs-人造膜鑲嵌模型重構。
2.1脂質體(liposome)
脂質體是將兩性分子如磷脂和鞘脂分散于水相,分子的疏水尾部傾向于聚集在一起,避開水相,而親水頭部暴露在水相,形成具有雙分子層結構的封閉囊泡。脂質體可由純脂質或混合脂質制備,其比例可根據目的蛋白進行調整。脂質體的大小可通過分散制備步驟進行調整,如膨脹[29]、擠壓[30]、乳化、超聲波、電形成[31]、噴墨形成和凍融循環等。對于MPs中的轉運體如核苷轉運蛋白,脂質體有其獨特的優勢。重組脂質體可以通過選擇性濃縮脂質體內底物對MPs進行功能完整性測試。同樣,如果蛋白脂質體是在底物存在下形成,也可以進行反向評估[32]。此外,脂質體中脂質的比例和種類會極大的影響MPs的活性、穩定性和結晶性能[33]。脂質體可以通過穩定蛋白質折疊、單體和亞單位之間的聯系來促進結晶,也可以通過脂質體介導的晶格接觸來促進結晶,從而測定MPs的結構和功能以及相應的藥物靶點研究。Kurisu等[34]發現與傳統磷脂相比,加入非天然脂質二油酰基卵磷脂(DOPC)可以促進了藍藻細胞色素b6f復合體的結晶。Jidenko等[35]用洗滌劑/DOPC混合物溶解并結晶得到在酵母中過表達的哺乳動物Ca2+-ATP酶。
2.2雙胞體(bicelles)
雙胞體是由長鏈磷脂和短鏈脂質(或洗滌劑)混合形成的自組裝圓盤結構[36],長鏈磷脂形成含MPs的雙分子層,然后由位于雙分子層邊緣的短鏈脂質穩定。目前最常用的組合是二己酰磷脂酰膽堿(DHPC,短脂)和二肉豆蔻酰磷脂酰膽堿(DMPC,長脂)的組合。根據長脂與短脂的比例、溫度、pH值和鹽濃度的不同,雙胞體具有不同的構象。雙胞體是介于脂質體囊泡和經典洗滌劑膠束之間的一種中間形態,結合了這兩種系統的優點。與脂質體相比,雙胞體更容易實現均勻混合;與經典洗滌劑膠束相比,雙胞體中洗滌劑用量更低,并且更加接近天然的膜環境[37]。但雙胞體也有其局限性,如[DMPC]:[DHPC]的合適比例往往難以控制。在雙胞體中洗滌劑交換步驟有時會導致MPs的聚集,存在洗滌劑使用相關問題的限制。
2.3納米盤(nanodisc)
納米盤由磷脂和兩親性螺旋蛋白,也稱膜支架蛋白(membrane scaffold protein,MSP)組成。一般由130~160個磷脂形成含MPs的雙分子層,然后由MSP作為與MPs結合的疏水基團保持其天然構象[38]。單個MPs可形成150 kDa大小的納米盤。組裝納米盤時,首先將MSP按照一定比例與預先溶解在洗滌劑(通常是膽酸鈉)中的磷脂混合,孵育一段時間后利用透析或疏水吸附劑去除洗滌劑,隨后納米盤自行組裝形成納米級別類膜結構圓盤[39]。組裝包含MPs的納米盤只需在體系中再加入適量MPs,其自組裝過程與空納米盤相似。包含MPs的納米盤與空納米盤通過生化手段進行分離,隨后用分子排阻色譜進一步純化,過程如圖2所示[40]。
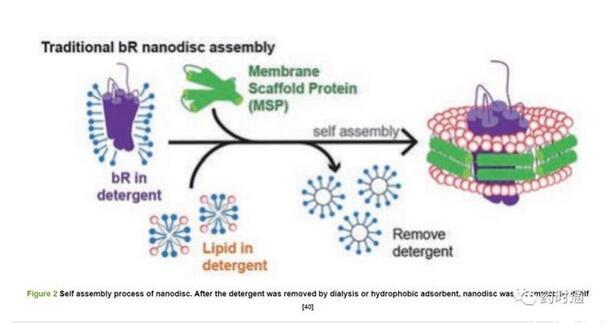
對于MPs的穩定分離純化而言,納米盤體系可以在溶液中提供類膜環境,它具有和細胞膜一樣的脂質組成。與其他人造膜相比,MSP的添加可以更好地穩定MPs的天然構象。應用納米盤開展的MPs研究較廣泛,GPCR家族蛋白β2AR被證明在納米盤體系中可以保持蛋白的結構完整和功能活性[38]。此外Yao等[41]使用納米盤研究B細胞淋巴瘤/白血病基因表達的抗凋亡蛋白(BCL-XL)在其膜環境下的構象和功能,結果顯示納米盤并未改變BCL-XL的N端的球狀結構,并且增強了其BH3配體的結合活性。針對傳統的納米盤的構型,Nasr等[42]設計了共價環化納米盤(covalently circularized nanodiscs,CNDs),其較傳統納米盤具有更高的穩定性、可控的直徑和形狀可調等優點,被應用到電壓依賴性陰離子通道蛋白-1(VDAC-1)和G蛋白偶聯受體-NRT1上。
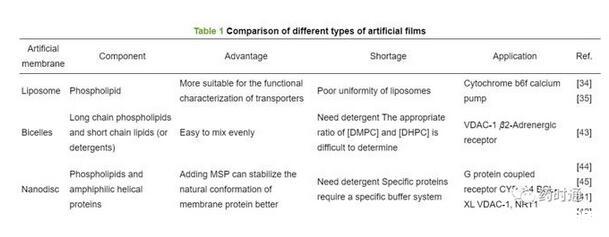
與雙胞體一樣,納米盤的第一步是基于洗滌劑的增溶,需要優化所使用的洗滌劑的性質和濃度,這在納米盤重組中可能造成蛋白質活性損失,因此同樣存在洗滌劑使用相關問題的限制。表1[34,35,41-45]比較了脂質體、雙胞體、納米盤的組成及其優缺點。
03、聚合物穩定技術
針對洗滌劑和人造膜分離純化和穩定MPs的不足,研究人員從保護MPs周圍局部脂質環境的思路出發,開發出了完全不添加洗滌劑的新方法,采用包括苯乙烯馬來酸、二異丁烯馬來酸、聚甲基丙烯酸酯等聚合物來穩定含有MPs的納米級脂質圓盤。
3.1苯乙烯-馬來酸酐(styrene maleic anhydride,SMA)聚合物
SMA是苯乙烯和馬來酸酐通過自由基聚合得到一種性能優良的共聚物,該聚合物由親水性的馬來酸和疏水性的苯乙烯交替組成[46]。SMA和大約140個脂質組成苯乙烯-馬來酸酐脂質顆粒(SMA lipid particles,SMALPs)[47]。組裝SMALPs時,首先將細胞懸液破碎處理,然后將一定量SMA添加到pH值≥6.5的細胞破碎懸液中,孵育一段時間后可發現該混合體系變澄清,表明SMALPs自組裝完成[48],接下去采用光散射技術來檢測SMALPs組裝完成后的物理參數。Xue等[49]通過研究SMALPs自組裝過程發現,SMA共聚物首先將末端的苯乙烯基團結合到膜表面,隨后疏水相互作用驅動苯乙烯基團插入脂質雙分子層的中心。當SMA共聚物的疏水側鏈完全插入時,局部脂質雙分子層產生波動,形成小的跨膜孔。隨著跨膜孔生長,SMA將羧基定向到跨膜孔上,并且在脂質尾部之間插入苯基來穩定邊緣,從而完成SMALPs自組裝,SMA提取純化膜蛋白過程如圖3所示[50]。
目前SMA方法已經成功地應用于穩定和分離純化離子通道蛋白[51]、轉運蛋白[51]、酶[52]、呼吸鏈復合物[53]以及受體[54]等。當苯乙烯與馬來酸的比例為2∶1或3∶1時,SMA對MPs的分離純化效果最好。另外SMA的提取效率還受到目標蛋白的大小和蛋白在膜中的包裹密度的影響[46]。與洗滌劑和人造膜相比,SMA的優勢在于其通過SMALPs的自發組裝將目標蛋白與天然脂質雙分子層以及相關蛋白一起提取。這不僅提供了相關蛋白與目標蛋白相互作用的信息,而且還提供了一種識別目標蛋白周圍內源性脂質組成的方法。此外,純化成SMALPs的MPs具有顯著的穩定性,在4℃時SMALPs至少能保持一周穩定,在經過幾輪凍融循環后,SMALPs顆粒完整性和蛋白功能損失最小[55]。
但SMA對低pH和二價陽離子不耐受的特點限制了該策略在MPs下游研究中的應用[56,57],因此人們對SMA進行結構修飾,合成SMA-ED、SMAd-A[58]和SMI[59]等pH值可調和耐受二價陽離子的聚合物脂質納米盤,有望成功應用于MPs的穩定提取上。
3.2二異丁烯-馬來酸(diisobutylene maleic acid,DIBMA)聚合物
SMA對二價陽離子耐受性低,限制了Mg2+和Ca2+等陽離子的使用,而這些陽離子通常用于蛋白質純化和活性測定的緩沖液中。最近有研究表明,二異丁烯-馬來酸(DIBMA)共聚物也能夠直接溶解膜,形成DIBMA脂質顆粒(DIBMALPs),可以克服上述SMA局限性。Oluwole等[60]發現DIBMALPs比SMALPs對二價陽離子如Mg2+耐受性更高。當Mg2+濃度超過4 mmol·L-1時,SMALPs內的蛋白質開始聚集變性,在Mg2+濃度為8~10 mmol·L-1時蛋白質全部失活。但在DIBMALPs中,當Mg2+濃度為10 mmol·L-1時,只有20%的蛋白質變性失活。Danielczak等[61]研究發現當使用DIBMA時,添加Mg2+或Ca2+可以提高提取效率。盡管DIBMA對于某些MPs的提取純度和穩定性要比SMA低,但DIBMA對二價陽離子有更高的耐受性,可以為蛋白質構象和動力學的研究提供了更好的環境[62]。因此,選擇哪種聚合物取決于所研究的目標蛋白的特征。
3.3聚甲基丙烯酸酯(polymethacrylate,PMA)聚合物
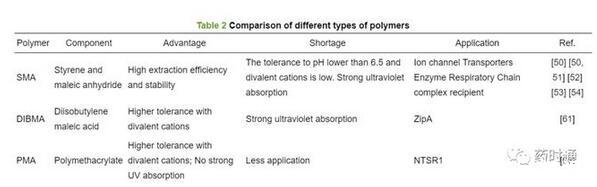
盡管SMA和DIBMA在一些MPs的分離純化中取得了成功[63],但存在SMA對二價陽離子耐受性低、DIBMA提取純度和穩定性低的缺陷并且這兩種聚合物都有強烈的紫外吸收,可能干擾紫外檢測[57]。因此人們開始尋找非“烯烴-馬來酸支架”替代聚合物。最近,兩親性聚甲基丙烯酸酯聚合物(polymethacrylate,PMA)被證明可將脂質雙分子層溶解成納米圓盤。PMA比常見的苯乙烯-馬來酸聚合物具有潛在的優勢,但目前PMA對于MPs的純化應用較少[64]。Lavington等[63]以神經緊張素受體1(NTSR1)為對象,探索使用PMA的無洗滌劑純化。通過使用Sf9細胞中表達的NTSR1-eGFP融合蛋白,篩選了一系列的增溶條件,證明了溫度、pH、NaCl濃度以及聚合物和膜樣品的相對數量的重要性。此外還發現PMA對二價陽離子有一定耐受性。PMA溶解的NTSR1比洗滌劑溶解的NTSR1表現出更大活性,這表明PMALPs為NTSR1提供了更天然的膜環境[63]。因此,PMA是一種可替代SMA的MPs純化方法,在研究NTSR1和其他MPs方面具有良好的前景。表2比較了SMA、DIBMA、PMA的組成、優缺點及其應用。
04、慢病毒載體穩定技術
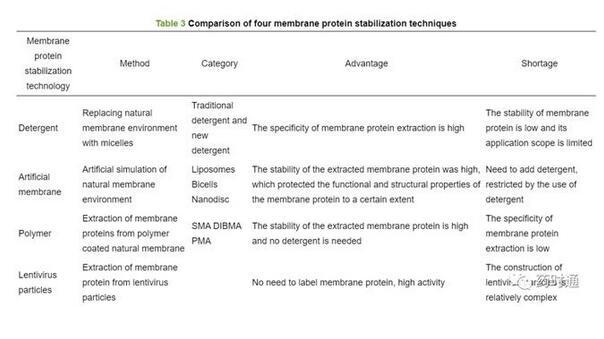
慢病毒(lentivirus)載體是以人類免疫缺陷I型病毒(HIV-1)為基礎發展起來的基因載體。慢病毒載體可以將外源基因或外源的shRNA有效地整合到宿主染色體上,從而達到持久性表達目的基因的效果。基于慢病毒顆粒(lentivirus particles,LVPs)作為MPs載體的策略是將目的基因插入慢病毒轉染所需的質粒當中,慢病毒從包裝細胞出芽的過程中會攜帶包裝細胞的細胞膜片段,從而獲得細胞膜上的MPs[65]。這種慢病毒穩定策略具有以下優點:①慢病毒顆粒表面的MPs受體表達水平高,活性高;②慢病毒顆粒可以直接固定在芯片上,無需標記;③慢病毒顆粒易于表達和純化。因此,基于慢病毒顆粒的穩定策略在研究MPs與配體之間的相互作用方面有巨大潛力,Heym等[11]將慢病毒顆粒結合表面等離子體共振(surface plasmon resonance,SPR)和表面聲波技術應用于GPCR與其配體(CXCR4抗體-12G5、AMD3100)的結合動力學研究。結果顯示,該方法得到的動力學參數和親和參數,與經典的細胞親和實驗測量值一致,為靶向GPCRs的小分子動力學分析提供基礎。此外,Hoffman等[66]構建LVPs-SPR體系來研究趨化因子受體4(cx-chemokine receptor 4,CXCR4)與其配體的相互作用。以293T細胞為宿主,構建了高/低表達CXCR4的慢病毒顆粒,并將其偶聯在Biacore F1芯片上進行CXCR4的抗體親和力評估。表3總結比較了上述MPs穩定技術的原理、分類以及優缺點。
05、MPs穩定技術結合表面等離子共振技術在藥物篩選中的應用
MPs配體藥物篩選和MPs的生物標志物發現是目前新藥研發的重要方向。據統計在DrugBank數據庫中,已批準的藥物靶點中有54%是MPs。截至2017年,FDA批準的分子靶標中只有667個是蛋白質,而在DrugBank數據庫中的MPs靶標總數為3 041個[2,67]。可見,批準的MPs靶標數遠少于MPs靶標總數。MPs的低表達量以及強疏水性等特點限制了MPs靶標的體外研究以及配體藥物篩選。因此,MPs穩定技術結合表面等離子共振技術的發展給眾多待開發的潛在MPs靶標和相關配體藥物篩選帶來了曙光。
目前針對MPs的配體高通量篩選技術中最具代表性的是SPR。它是一種敏感的表面分析技術,它是通過分子吸附在重金屬膜上引起介電常數的變化來進行檢測,自20世紀90年代以來,這種方法被廣泛用于簡單的蛋白配體以及小分子藥物的高通量篩選[68]。Johzuka等[69]建立了高精度表面等離振子共振(HP-SPR)-3D系統,它能在加藥1 h內對抗癌藥物進行模擬體內表型篩選。Wang等[70]模擬了PD-1/PD-L1在蛋白質-蛋白質界面上的潛在結合區域,在內部肽庫中結合虛擬篩選和SPR親和力評估,得到三種PD-1靶向肽抑制劑。此外,SPR也成功應用于表皮生長因子受體的配體[71]、泛素化抑制劑[72]、IL-6家族細胞因子受體GP130 PPI抑制劑[73]的篩選。
然而,對于GPCR、ABC轉運蛋白等表達量低且結構復雜的多次跨MPs,當它們直接與固體底物特別是Biacore系統中的金底物接觸時,MPs通常會失去功能或變性。所以,研究者們引入MPs穩定技術獲得活性良好的MPs,再與SPR結合用于其相應的配體藥物的篩選。Komolov等[74]將洗滌劑穩定化的視紫紅質蛋白偶聯于SPR芯片表面,成功用于分析視紫紅質蛋白與其配體間的相互作用。與經典的洗滌劑策略相比,人造膜穩定策略結合SPR技術在MPs配體篩選以及新藥研發中應用更為廣泛。Oshima等[75]將包裹有hERG通道蛋白的人工雙層脂質膜重建在硅芯片的微孔中,評價了這個體系的耐用性,隨后Tadaki等[76]優化了該組裝過程,Komiya等[36]根據優化后條件,將該系統定量評價西沙必利對細胞合成hERG鉀通道的作用。結果發現用該體系測得的IC50與膜片鉗法測量值一致,最終建立了作用于hERG鉀離子通道的藥物快速篩選平臺。Das等[45]將納米盤穩定技術和局域表面等離子體共振技術(LSPR)結合,用于分析12種小分子藥物與細胞色素P450 3A4酶的結合類型。結果顯示,溴隱亭、睪酮、洛伐他汀、阿德司瓊、α-萘酚酮、紅霉素和硝苯地平為I型藥物,通過取代配位水分子來調節酶活性;酮康唑、伊曲康唑、曲酰環丙胺、雙氯芬酸和特非那定為II型藥物,通過直接與鐵結合來抑制酶。Maynard等[77]為解決GPCR配體篩選方法的局限性,首先用脂質雙分子層將GPCR分離純化,隨后通過納米孔將其固定在芯片上,用SPR技術采集GPCR配體結合的劑量-反應曲線,建立了GPCR配體的高通量篩選平臺。Rich等[78]以SPR技術建立了CCR5蛋白最佳的增溶條件篩選體系,以抗體Fab(2D7)為陽性藥,在96種不同的洗滌劑中找出既能有效溶解受體又能保持其活性的洗滌劑,結果顯示大多數保持CCR5活性的去污劑是帶有C9到C13烷基尾的麥芽糖,而短(≤C8)或長(≥C14)烷基鏈的麥芽糖是無效的增溶劑。Xu等[79]采用納米圓盤穩定的離子通道蛋白KcsA-Kv1偶聯于SPR芯片上,用于分析KcsA-Kv1蛋白及其抑制劑間的相互作用。
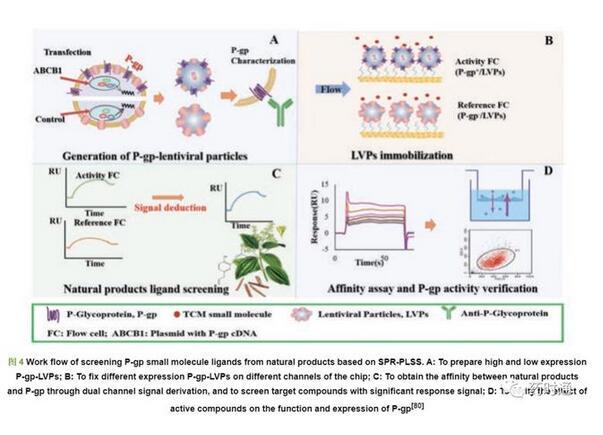
針對慢病毒載體穩定技術結合SPR在中藥活性成分篩選中的應用,本課題組已展開一些探索性研究。P-糖蛋白(P-gp)是體內最重要的外排型轉運蛋白,具有12次跨膜的復雜結構,且尚未商品化。Cao等[80]采用LVPs穩定策略,獲得活性良好的P-糖蛋白,構建了一種基于SPR的P-糖蛋白配體篩選系統。首先,獲得P-gp高表達和低表達的LVPs,然后將P-gp高/低表達的LVPs分別固定在CM5芯片上作為活性通道和參比通道。以P-gp抑制劑伐司樸達(valspodar,Val)和環孢素(cyclosporin,CsA)為陽性對照,從天然產物庫中快速篩選出厚樸酚、和厚樸酚和白藜蘆醇作為潛在的P-gp配體(圖4)[80]。Chen等[81]構建了CXCR4的配體篩選體系,將高/低表達的CXCR4的慢病毒顆粒固定在CM5芯片上,以趨化因子受體拮抗劑AMD3100為陽性化合物,從川芎提取物中篩選出洋川芎內酯Ⅰ為CXCR4的潛在配體。
MPs穩定技術在面向結構復雜的MPs的藥物篩選中是不可缺少的關鍵技術,它能夠模擬MPs所需的天然脂質環境,保證MPs結構和功能的完整性,為建立高專屬性、高靈敏度和高通量的藥物篩選方法提供技術支撐。
06、小結與展望
MPs功能的完整性對于藥物靶點的發現和新藥研發至關重要,而MPs的穩定技術是保障其基本功能完整性的關鍵。本文總結了近年來MPs穩定技術的發展。最初研究人員利用洗滌劑膠束來分離MPs,但此方法忽略了天然脂質環境對MPs結構和功能的獨特作用;人造膜穩定技術有助于模擬MPs天然的功能和結構,但在人造膜組裝過程中仍然需要應用洗滌劑增溶,未能避免洗滌劑應用中產生的問題;目前最新的聚合物穩定技術在完全無洗滌劑的環境下可以將目的蛋白與天然脂質雙分子層一起分離,使其保持天然的膜環境,能在最大程度上減少MPs結構和功能的缺失;而慢病毒顆粒穩定策略無需處理就能直接與SPR芯片結合,使得其在下游應用特別是與SPR聯用上有其獨特優勢。然而上述這些策略仍然存在一些技術難點,包括如何增加MPs提取的特異性,如何減少MPs提取過程中帶來的結構和功能的缺失,需要更全面的MPs功能驗證來確保所建立的方法的準確性。因此,研究人員一直致力于開發新型MPs穩定技術,以期在維持MPs正確結構的前提下獲得純度較高的目標MPs。盡管MPs穩定技術在藥物篩選中已聯合SPR技術有了一些應用,但今后仍需拓寬其應用范圍,以更好地服務于藥物靶標發現與配體篩選。MPs的穩定是藥物研究中亟待解決的科學問題,開發特異性強、效率更高的新型MPs穩定技術任重而道遠。
作者貢獻:方家豪負責文獻檢索及論文撰寫;曹雨虹負責修改文章;何宇臻負責修改文章;洪戰英負責文章選題、指導寫作、修改及校對文章。柴逸峰負責審閱文章。
利益沖突:本文無利益沖突。
作者:方家豪,曹雨虹,何宇臻,洪戰英柴逸峰
機構:海軍軍醫大學藥學院,上海200433
來源:藥學學報,2021,56(9):2325-2334.










