合作客戶/
拜耳公司 |
同濟大學 |
聯合大學 |
美國保潔 |
美國強生 |
瑞士羅氏 |
相關新聞Info
為什么水滴最終是保持球形的?
來源:佛系的何大大 瀏覽 961 次 發布時間:2022-06-22
先上結論:因為水的?表面?存在張力?。
?分子間作用力
要理解水的表面張力,先要明確這么一個概念:分子間作用力。
分子間作用力,又稱范德華力(van der Waals force)。是存在于中性分子或原子之間的一種電性吸引力。分子間作用力有三個來源:①極性分子的永久偶極矩之間的相互作用。②一個極性分子使另一個分子極化,產生誘導偶極矩并相互吸引。③分子中電子的運動產生瞬時偶極矩,它使鄰近分子瞬時極化,后者又反過來增強原來分子的瞬時偶極矩;這種相互耦合產生靜電吸引作用,這三種力的貢獻不同,通常第三種作用的貢獻最大。
———《中國大百科全書》總編委會.《中國大百科全書》.《中國大百科全書》出版社,2009
關于分子間作用力的組成、產生原因等十分復雜,今天并不去過多介紹。不過我們需要了解的是,在分子間作用力的影響因素中,分子間距是極其重要的一個。兩者具體的關系如下圖所示:
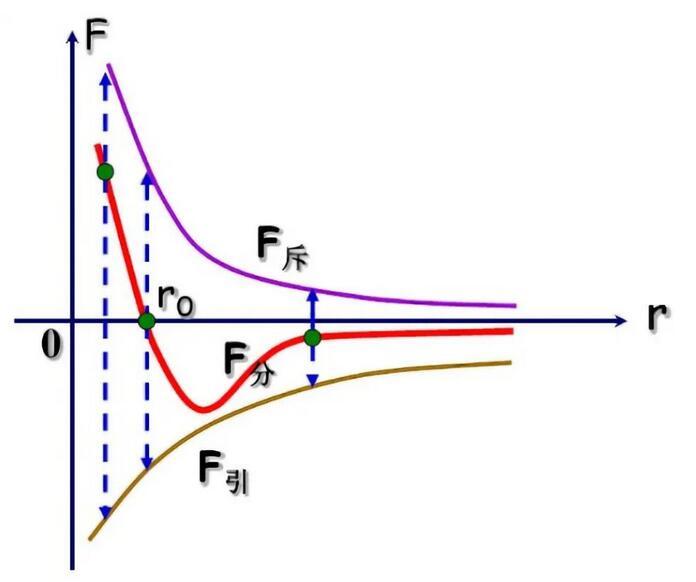
分子間作用力隨分子間距變化曲線
從圖中我們可以觀察得到:分子間距較小時,分子間作用力表現為斥力;分子間距較大時,分子間作用力表現為引力。
?水的表面張力
在水的內部,分子間距普遍大于上圖?中?的?r0,于是平時,各個水分子之間互相拉著對方,平安無事。
但在水的表面情況就不一樣了,表面的水分子只受到內部的其他水分子向里的拉力,所有水分子爭先恐后向里擠的結果就是使整個水滴呈現一個球形。

球形水滴
就好比?橄欖球比賽?,當?所有人?都想?搶中間?的?球?,每個人?都想?往?中間擠?,最終?大家?一定會?呈現?一個圓形?。
那么問題來了?,為什么表面的水分子只收到向里的拉?力呢?兩個原因:
表面的水分子外面只有空氣分子,而空氣分子之間隔的太遠了,以至于分子間作用力基本為零,無法影響到表面的水分子;
表面的水分子太活潑,許多都躍出了水面,導致表面水分子減少,更加抵擋不住內部水分子的吸引力。
這就是水滴是球形的原因啦。
?浸潤和不浸潤
水表面張力能解釋的現象有很多,比如清晨荷葉上的露珠,比如毛細現象。又或者?中學化學都學到過試管內的水液面并不是水平的,而是向下凹陷的。
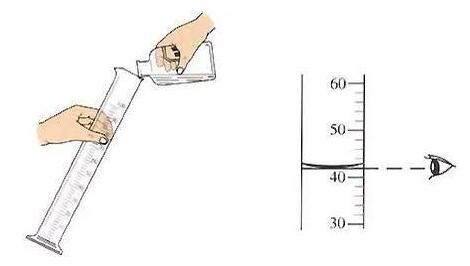
視線與凹液面最低處水平
這是為什么呢?按照剛才的理論,水想要變成球型,上液面不應該是凸出來的嘛?
這是因為水對于玻璃來說是浸潤液體,即玻璃分子喜歡和水分子在一起。兩個人關系好,拉力強,所以器壁附近本該被內部水分子拉下去的表層水分子,在器壁的拯救下留了下來,相應的,中間的水分子沒有器壁的拯救,就自然凹了下去。
那有沒有玻璃分子不喜歡的人呢?當然,水銀分子相對于玻璃就是非浸潤液體,所以我們會觀察到,沒有器壁玻璃分子的拉力,試管內的水銀液面就?是凸出來的。
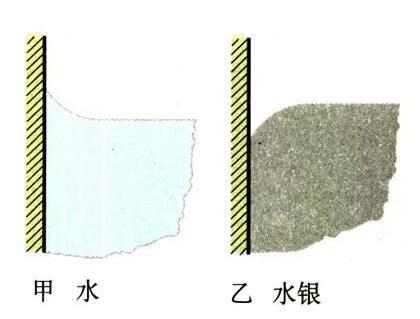
水液面和水銀液面
好了,這就是水表面張力的解釋,如有錯誤還請指正!










