合作客戶/
拜耳公司 |
同濟大學 |
聯合大學 |
美國保潔 |
美國強生 |
瑞士羅氏 |
相關新聞Info
Delta-8調整表面活性劑的質量比實現類似于帶電荷的聚合電解質-表面活性劑混合體系的相分離(下)
來源:上海謂載 瀏覽 679 次 發布時間:2022-06-13
結果和討論
聚二烯丙基二甲基氯化銨(pDADMAC)。表2給出了研究中使用的pDADMAC樣品的分子量表征。
表2:pDADMAC聚合物分子量的測定
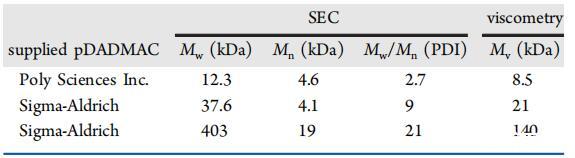
所有情況下的SEC色譜圖均為具有不同多分散性的單峰色譜圖。隨后用于定義聚合物的粘度平均分子量Mv使用庫恩法獲得?做記號?毫溫克?櫻田關系η=KMa,常數K=4.71×10?3,指數α=0.83,是類似實驗條件下一系列參考文獻的平均值。19?21
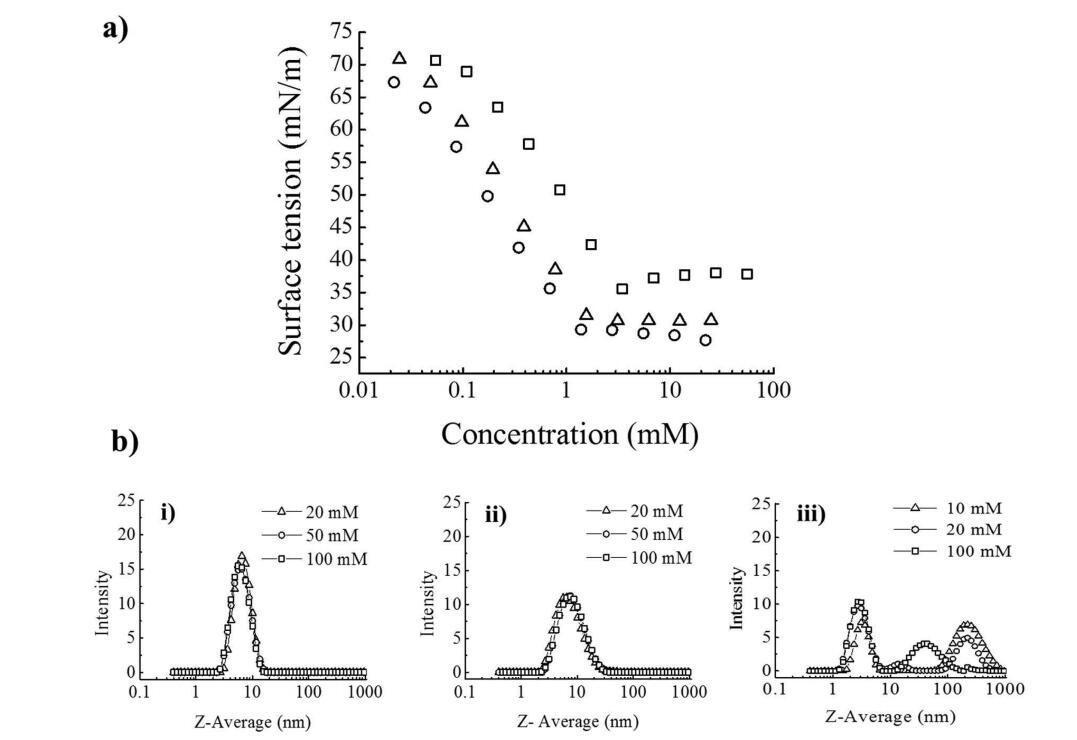
圖1:。(a)25°C水中的表面張力曲線(□)美國銀行(○)DDQ和(Δ)BAC/DDQ(2:3 mol/mol)。(b)25°C下的PCS強度曲線隨濃度變化:(i)BAC(0.3 M NaCl),(ii)BAC/DDQ 2:3 mol/mol(0.05 M NaCl),和(iii)DDQ(5×10?3 M NaCl)。
季銨鹽氯化物表面活性劑。測定了純表面活性劑和BAC/DDQ(2:3mol/mol)的表面張力曲線,由于其最近報告的在抗菌制劑中的有益性能,因此選擇了特別關注的表面活性劑和BAC/DDQ(2:3mol/mol),22(圖1a)。使用吉布斯吸附等溫線17(表3)測定cmc和計算的每個頭基表面積,BAC和DDQ都具有可比的頭基表面積。對于BAC,這是由于BAC中所含的苯基基團朝向季銨鹽頭基旁邊,而不是膠束內部,從而形成更大的頭基23?27而在DDQ中,表面活性劑的兩個癸基尾部會導致更大的尾部填充,從而限制表面活性劑在空氣中有效吸附的能力?水界面。
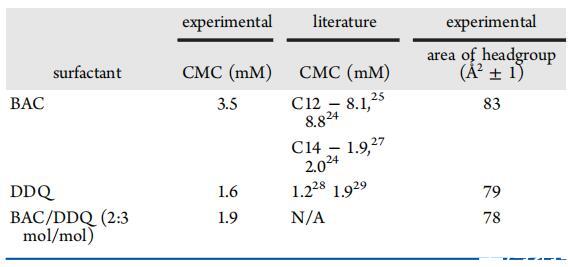
表3:。空氣中BAC、DDQ和BAC/DDQ 2:3 mol/mol的表列CMC和每人頭群表面積值?25°C時的水界面
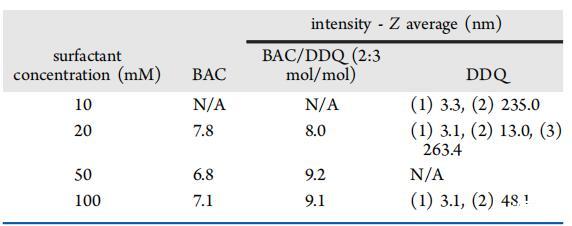
光子相關光譜(PCS)用于測定膠束的流體動力學直徑。BAC和BAQ/DDQ 2:3 mol/mol的PCS分布圖(圖1b)顯示了在相關濃度范圍內的單峰分布,平均Z平均值和單峰分布表明存在橢球或球形膠束幾何結構。DDQ呈現雙峰/三峰分布,表明膠束結構具有較大的聚集數(表4)。這可以用具有徑向長度和軸向長度的圓柱形幾何體或與單分子或多分子囊泡平衡的球形膠束來解釋。28這兩種情況與早期DDQ熒光探針研究的結果一致,該研究觀察到膠束聚集數從20增加到86,濃度從10增加到81 mM。29
表4:。表中PCS Z-25°C下各表面活性劑的平均值
p(DADMAC)與DDQ和BAC混合物的相分離。為了量化每個系統內相分離所需的臨界離子強度,制備了一系列含有100 mM(~3.6 wt%)表面活性劑加上不同濃度的聚電解質,包括通過比較NaCl和系列內第一個樣品對相分離的影響。構建了相分離邊界圖,以說明8.5 kDa pDADMAC/DDQ的非相分離和相分離混合物之間的相邊界(圖2a),圖2b所示為相分離行為示例。
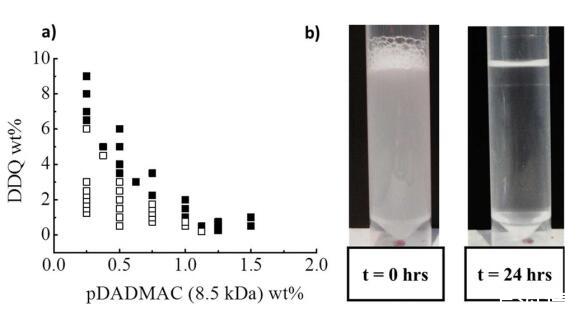
圖2:。(a)25°C下pDADMAC(8.5 kDa)/DDQ/水的相分離邊界:(□)單相和(■)兩個階段。(b)樣品pDADMAC(3 wt%)/DDQ(3 wt%)/水的相分離圖像(t=自上次攪拌以來的時間)。
對于表現出分離相分離的選定pDADMAC/表面活性劑/水混合物,在最后一次攪拌24小時后從頂部和底部相中取小份。測量每個相的體積,并計算預測重量百分比,假設兩相之間完全分離。進行了重量分析,表明頂部相較濃,底部相較稀。在表5中,pDADMAC 8.5 kDa(3 wt%)/DDQ(3 wt%)/水的預測和實際重量百分比值雖然非常一致,但在統計上不具有可比性。1 H NMR(圖3)表明,上相富含表面活性劑,而下相富含聚電解質,這與早期的研究一致。11因此,術語“富含表面活性劑層”和“富含聚電解質層”將用于描述不同的相。
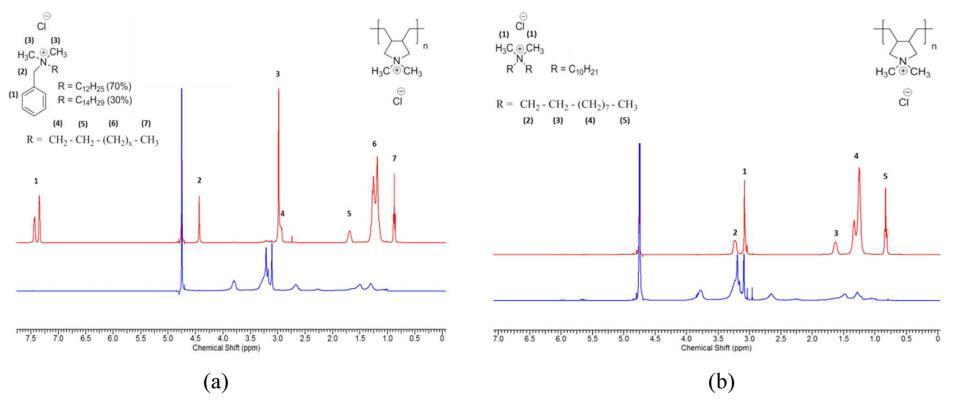
圖3:。樣品頂相和底相的1 H NMR:(a)pDADMAC 8.5 kDa(3 wt%)/BAC(3 wt%)/水樣和(b)pDADMAC 8.5 kDa(3 wt%)/DDQ(3 wt%)/水樣,自上次攪拌后24 H。(紅色)頂相(表面活性劑)和(藍色)底相(pDADMAC)。
表5:。最后一次攪拌后24小時pDADMAC 8.5 kDa(3 wt%)/DDQ(3 wt%)/水的頂層和底層重量分析

對于所研究的表面活性劑和表面活性劑混合物,將pDADMAC的分子量從8.5增加到140 kDa對相分離邊界的影響可以忽略不計(圖4a)。
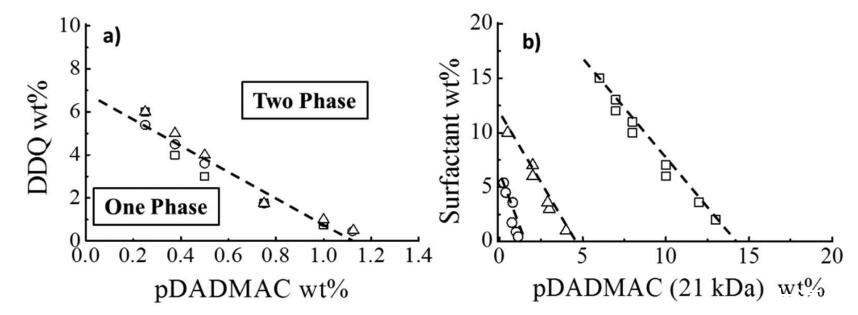
圖4:。(a)pDADMAC/DDQ/水的相分離邊界作為pDADMAC分子量的函數:(□)8.5 kDa(○)21 kDa和(Δ)140 kDa(25°C時)。(b)pDADMAC的相分離邊界(21 kDa)/表面活性劑/水(○)DDQ(□)25°C下的BAC和(Δ)BAC/DDQ(2:3 mol/mol)。虛線表示相界的大致位置。
與BAC相比,在恒定聚電解質分子量條件下,DDQ相分離濃度低得多時,對表面活性劑型相分離邊界的影響更為顯著,以BAC/DDQ(2:3 mol/mol)為例的混合物系統地處于兩個極端之間(圖4b)。應注意的是,BAC的張力測定曲線顯示cmc周圍存在最小值,這表明存在雜質,常見的解釋是存在疏水性共溶劑,即長鏈醇。如前所述,長鏈醇可以增加聚電解質/表面活性劑的相容性,但其濃度對其影響很小。為了充分研究BAC/DDQ表面活性劑比對相界的影響,在恒定的表面活性劑濃度(100 mM)下配制了一系列混合物≈3.6 wt%),不同pDADMAC(21 kDa)濃度,并與不同NaCl濃度進行比較。相分離系列中的第一個樣品被確定為該系統的相分離濃度(圖5)。
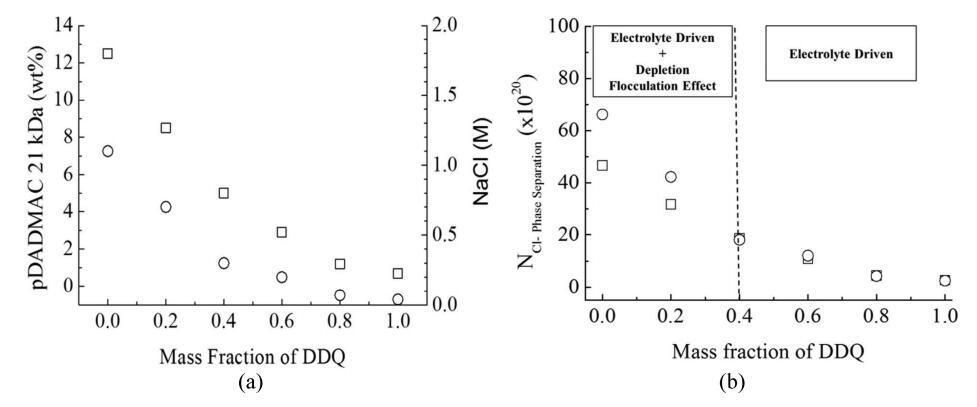
圖5:。(a)臨界相分離濃度與BAC/DDQ質量比的函數關系。表面活性劑(BAC/DDQ)濃度保持恒定(100 mM≈3.6 wt%):(○)NaCl和(□)pDADMAC(21 kDa)。(b)誘導相分離所需的電解液中氯離子的數量(NCl?相分離)作為BAC/DDQ比的函數。表面活性劑(BAC/DDQ)濃度保持不變(100 mM/≈3.6 wt%)。電解液類型:(○)NaCl和(□)pDADMAC(21 kDa)。
觀察到顯示分離相分離的NaCl/表面活性劑/水混合物,以產生富含表面活性劑的上層相,類似于聚電解質/表面活性劑/水混合物中的相分離。這說明,對于pDADMAC(21 kDa)和NaCl系統,可以通過改變BAC/DDQ的比率來控制相界。
討論
可以直接比較臨界pDADMAC和NaCl相分離濃度與電解質摩爾數的關系;因此,氯離子的數量(NCl?計算了相分離所需的相分離(表6)。在圖5b中,我們比較了NCl?pDADMAC和NaCl系統的相分離是DDQ質量分數的函數。我們發現,對于DDQ質量分數大于0.4的表面活性劑混合物,無論是NaCl還是聚電解質,分離相分離所需的離子強度都是相同的。我們將這種電解質驅動力歸因于表面活性劑季銨鹽頭基周圍的離子氣氛,其尺寸減小,導致反離子冷凝。相分離后,表面活性劑不溶于水,形成不混溶油,由于其密度低,將奶油狀至溶液頂部,并聚結形成富含表面活性劑的相。由于聚電解質濃度的減少/減少,表面活性劑分子在這種富含表面活性劑的相中變得可溶,因此頭基周圍的離子氣氛增加。根據所提供的數據,不可能確定季氮周圍的還原離子大氣是否足以單獨誘導相分離,或者是否形成了真正的親密離子對。親密離子對是指帶電部分(在本例中為季銨鹽基團)與其對應的反離子直接接觸,隨后中和離子電荷,需要對這方面進行進一步研究,以充分闡明其機理。
我們認為,含有較大質量分數DDQ的表面活性劑混合物需要較低的離子強度來誘導相分離,這是因為表面活性劑DDQ和BAC的膠束性質不同。文獻中已經注意到,與球形膠束相比,圓柱形膠束在膠束結構中的反離子離解度較小,其背后的原因是,與圓柱形幾何相比,球形幾何中表面活性劑頭基之間的距離較大。30?32 PCS結果表明,在所研究的濃度范圍內,BAC膠束為橢球/球形,與DDQ膠束相比,膠束尺寸發生了名義變化,DDQ膠束為圓柱形或球形膠束和囊泡結構的組合。兩種表面活性劑膠束反離子離解常數的差異可能是上述混合物中誘導相分離所需的不同臨界離子強度的主要因素。
表6:。顯示氯離子數量的列表結果(NCl?)通過電解液添加到三元混合物中以誘導相分離a
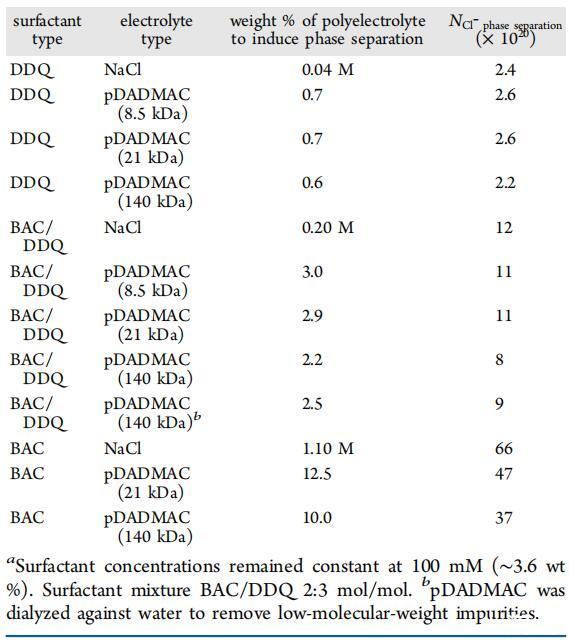
當DDQ的質量分數小于0.4時,在NaCl和pDADMAC系統之間觀察到偏差,聚電解質系統在較低的離子強度下誘導相分離,pDADMAC分子量越高,效果越明顯。為了進一步探索這種效應,在恒定的表面活性劑總濃度下,在BAC/DDQ比率范圍內研究了一系列不同分子量的pDADMAC分子。確定臨界相分離濃度,然后進行NCl?計算了相分離。這可以解釋為一種互補的耗盡絮凝效應,在這種情況下,聚電解質不吸附在表面活性劑膠束上,膠束熵耗盡相互作用可誘導相分離。熵虧損相互作用是由于聚合物鏈構象熵的變化導致的,這可以防止聚合物過于接近膠束。因此,當兩個膠束足夠緊密以防止聚電解質將其分離時,膠束之間的區域稱為聚合物耗盡。膠束間耗盡區外的聚電解質誘導滲透壓將膠束推到一起,并鼓勵溶液混合物內的相分離。11,33大量研究表明,在膠體中?類似電荷和低鹽度的聚合物混合物在比中性體系低得多的濃度下觀察到增強的耗盡相互作用。長程排斥靜電力被發現是這種增強的耗盡相互作用的背后,據報道溶劑的德拜長度是一個主要因素。還注意到,在較高電解質濃度下,聚合物的回轉半徑成為增加耗盡力范圍的一個重要因素。34?37對于本文研究的pDADMAC混合物,對于含有較低DDQ質量分數的混合物,提議的耗盡效應更為顯著。在較高分子量下,耗盡效應也更為明顯,據報道,在1 M NaCl中8.8 kDa pDADMAC的回轉半徑為8.6 nm38,而114 kDa pDADMAC的回轉半徑為64 nm。19我們推測這是因為這些混合物更加集中。在濃度更高的混合物中,預計德拜長度會更小,但熵相互作用會變得更為主導,并預計會增加耗盡相互作用。
結論
在本文中,我們提出了一種類似帶電季銨聚電解質/表面活性劑/水混合物的分離相分離機制,該機制是由離子表面活性劑的季氮和氯化物反離子之間的離子大氣中的還原以及額外的聚電解質耗盡絮凝效應引起的。表面活性劑類型的性質是決定分離相分離開始的主要因素。對于BAC質量分數較高的混合物,有跡象表明存在額外的消耗絮凝效應,尤其是對于高分子量PDADMAC。據我們所知,這篇文章是第一篇報道調節likecharged聚電解質相分離點的能力?通過改變表面活性劑比率(BAC/DDQ)的表面活性劑混合物。
作者信息
通訊作者*電子郵件:stephen。yeates manchester.ac.uk.注:作者聲明沒有相互競爭的財務利益。
確認書
該項目通過EPSRC案例獎獲得資助,涉及曼徹斯特大學有機材料創新中心和Byotrol Plc的合作。我們還感謝B.Carter博士對利物浦大學材料發現中心的Epmotion 5075液體處理器(Eppendorf)和Kibron張力計的幫助。










